成都中医药大学中医药创新研究院/交叉学科研究院黎胜红/刘燕团队长期致力于药用植物活性萜类天然产物发现与生物合成研究。近期,团队系统性总结了光合蓝细菌作为微生物底盘可持续性生产植物源活性萜类天然产物的最新研究成果,深入剖析了代谢工程与合成生物学策略的应用突破,为该类高价值天然产物的绿色生物制造提供了全面的理论支撑与技术参考。相关成果以“Engineering phototrophic cyanobacteria as a robust platform for production of plant-derived bioactive terpenoids”为题,发表于《Chemical Engineering Journal》期刊(中科院一区,TOP期刊)。我校药学院2023级硕士研究生冯慧程和谭春林副教授为论文第一作者,我院引进人才刘燕教授、黎胜红教授和谭春林副教授为共同通讯作者。

萜类化合物(Terpenoids)是自然界中结构最丰富的天然产物家族,已鉴定种类超9.5万种,具有抗炎、抗癌、抗氧化等生物活性,在医药、食品、化妆品、生物能源等领域具有不可替代的应用价值。例如抗疟药物青蒿素、抗癌药物紫杉醇、抗氧化剂番茄红素等明星化合物均属于萜类家族。然而,传统生产模式面临严峻挑战:植物提取依赖有限的自然资源,产量低且破坏生态;化学合成存在立体选择性差、副产物多、环境污染等问题。开发基于微生物“细胞工厂”的绿色生物制造技术,已成为解决萜类化合物资源瓶颈的核心方向。
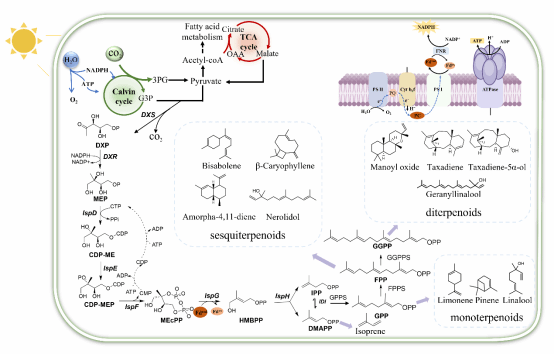
蓝细菌(Cyanobacteria)作为一类能够利用阳光和二氧化碳进行光合作用的原核生物,具备独特的天然优势:自带萜类前体合成的 MEP 途径,可直接将二氧化碳转化为异戊烯焦磷酸(IPP)和二甲基烯丙基焦磷酸(DMAPP);拥有丰富的类囊体膜结构和光合电子传递链,能为细胞色素P450酶(萜类后修饰关键酶)提供天然锚定位点和充足NADPH,解决了原核宿主中P450酶功能表达难题;无需有机碳源,可实现碳负性生物制造,契合全球低碳发展目标。此外,CRISPR-Cas9基因编辑、光响应启动子等成熟合成生物学工具的开发,进一步推动了蓝细菌底盘的改造应用。
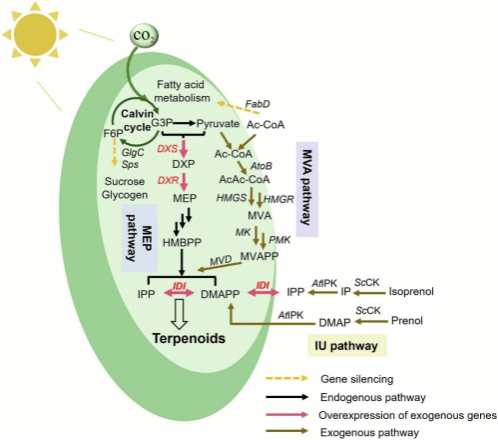
尽管优势显著,蓝细菌高效合成萜类仍面临多重瓶颈:碳代谢流分配失衡,超过80%的光合固定碳流向初级代谢,仅约5%进入萜类代谢;MEP途径的限速步骤存在菌株差异性,异源MVA途径引入又面临乙酰辅酶A供应不足和代谢负担等问题;萜类产物的细胞毒性及低浓度导致下游分离成本高昂等。针对这些关键问题,研究团队提出了多维度解决策略:通过酶工程优化萜类合酶与P450酶的兼容性和催化效率;改造MEP途径并引入异源前体合成途径,强化前体供应;利用CRISPRi/a、small RNA等技术抑制竞争途径,引导碳流定向分配;构建人工合成微生物群落实现跨物种分工协作;结合AI驱动的代谢建模精准预测优化靶点;通过原位产物提取、转运蛋白工程等缓解产物毒性。目前,这些策略已在蓝细菌中成功实现异戊二烯、柠檬烯、紫穗槐二烯等多种萜类化合物的合成,部分化合物产量已接近工业化评估阈值,展现出广阔的应用前景。
该研究不仅为利用蓝细菌细胞工厂异源合成植物源萜类化合物的理性设计与优化提供了系统的理论指导,也为其他高价值天然产物的生物制造提供了重要借鉴。
该研究得到国家自然科学基金(32400068,82222072)、四川省自然科学基金项目(2024NSFSC1833)、中国博士后基金项目(GZC20230332, 2024M750284, 2025T180738),四川省博士后创新人才资助项目(BX202318),成都中医药大学学生创新创业发展计划(S202510633013),植物化学与天然药物国家重点实验室开放项目(P2025-KF0X)资助。
全文链接:https://doi.org/10.1016/j.cej.2025.172487
(文、图/中医药创新研究院/交叉学科研究院)